随着人口老龄化的加剧,阿尔茨海默病(Alzheimer's Disease,AD)已成为全球范围内最常见的神经退行性疾病之一。其早期诊断和治疗对于延缓疾病进展、改善患者生活质量至关重要。近年来,随着Aβ单抗药物Lecanemab和Donanemab在中国相继获批上市,早诊早治的重要性愈发突出。
迪安诊断顺应这一趋势,重磅推出AD TANGO™系列产品,致力于为临床提供高性价比、高质量的检测服务,助力AD的早期筛查、诊断和全病程管理。
精准定位临床痛点
助力解决AD早期诊断难题
AD的早期诊断一直是临床面临的巨大挑战。早期症状不明显,且与其他神经系统疾病存在重叠,导致许多患者在确诊时已处于疾病中晚期,错过了最佳治疗时机。脑脊液检测和PET成像,虽然具有较高的诊断价值,但存在侵入性、费用高昂、检测不便等局限性。尽管国内外检测指标和技术手段众多,但针对AD两大核心指标Aβ42/Aβ40及p-tau217,能同时达到临床级应用的检测解决方案一直较为缺乏。因此,基于血液的非侵入性、高灵敏度、高特异性的早期筛查方法,对于AD的早期诊断、干预和治疗具有重要意义。
迪安诊断神经疾病与衰老检测(Targeting Neurology and Aging using Omics,TANGO)中心重磅推出的AD TANGO™系列产品精准定位这一临床痛点,通过多技术平台的优势互补和强强联合,实现了对AD血液生物标志物的高灵敏度和高特异性检测,提供了临床应用级的高准确度检测依据。
该系列产品适用于以下人群:
1.AD的辅助诊断:AD高风险人群,包括可疑的主观认知下降(SCD)群体、轻度认知障碍(MCI)患者和疑似痴呆患者。
2.AD的鉴别诊断:其他伴有认知障碍表现的神经系统疾病患者,如血管性痴呆、路易体痴呆、免疫性或感染性痴呆,以及部分与AD共病或增加AD风险的情况。
3.AD高风险遗传背景人群:如家族性AD基因突变携带者和散发性AD遗传高风险患者、年龄>50岁等,希望可以进一步了解自身AD风险的人群。
4.Aβ单抗用药指导及疗效监测:使用Aβ单抗药物(如Lecanemab或Donanemab)治疗前评估以及治疗过程中的人群。
5.其他需要脑脊液检测以外更高精度和准确度进行验证的情况,以及送检其他技术平台检测后仍有疑问的确认性复查。

打破技术平台壁垒
高性价比的“硬核、放心测”
AD TANGO™系列产品通过整合多技术平台,实现检测指标性能的优化配置,提供了堪称临床级检测的硬核方案,同时对疑难病例或是检测存疑报告提供了更佳的复查选择。AD TANGO™-2产品包括Aβ40、Aβ42、Aβ42/Aβ40、p-tau217四个检测指标,AD TANGO™-1产品则在AD TANGO™-2的基础上增加了ApoE基因分型检测。
1.基于IP-MS(免疫沉淀-质谱技术)检测Aβ42和Aβ40比值
Aβ42是AD疾病进程中最早出现的生物标志物,可在临床确诊前18年出现异常;而Aβ42/Aβ40比值的异常可出现于临床诊断前14年[1],这提示了其作为AD早期筛查生物标志物的巨大潜力。但一直以来,对Aβ42/Aβ40的检测,不同技术平台性能差异很大,且普遍性能不佳。这是由于Aβ40和Aβ42存在一定的技术检测难点(详见后述内容),而IP-MS技术在检测Aβ42/Aβ40方面显示出更优性能。
迪安诊断通过独家引进美国QUEST的IP-MS技术检测Aβ40和Aβ42,在检测血液Aβ方面性能卓越,对脑内Aβ病理预测的AUROC(受试者工作特征曲线下面积)可达0.862(95%CI 0.814-0.910)[2],通过参考区间的三分位划分,可对AD实现分层风险评估,在Aβ42/Aβ40≥0.17时,阴性预测值可达99%(95% CI 0.953-1.000)[3]。
Aβ42和Aβ40的检测难点
1 | Aβ42和Aβ40的结构极度相似,只有两个氨基酸的差异,只有特异性极高的抗体才能将两者区分出来。 |
2 | Aβ在血液中浓度很低,可达pg级别,需要高灵敏的检测技术。 |
3 | AD人群与非AD人群血浆中的Aβ42/Aβ40的差异只有10%~15%,要求检测技术进行精确定量,并具备良好的技术稳定性。 |
4 | Aβ与血浆中多种蛋白结合,基质效应可导致检测特异度降低。 |
IP-MS技术四大优势使得以上问题迎刃而解,实现Aβ40和Aβ42的精确定量。
优势一:高特异性的抗体富集技术提高检测特异性。
优势二:pg级检测下限,极高灵敏度。
优势三:直接且同时测定Aβ42和Aβ40降低的批内和批间差。
优势四:以稳定同位素标记的Aβ作为内标精确定义检测物质。
2.基于SimoA(单分子免疫阵列技术)检测高认可度的p-tau217
p-tau217与AD病理进程高度相关,与脑脊液检测和Aβ-PET具有高度一致性,可作为AD辅助诊断和鉴别诊断的重要指标。美国国家衰老研究所和阿尔茨海默病协会(NIA-AA)最新的《阿尔茨海默病诊断和分期的修订标准(2024年)》将其列为唯一可用于AD诊断的血浆指标。
SimoA技术平台的高灵敏度确保了即使在极低浓度下,也能准确检测p-tau217标志物水平,其在区分AD患者与健康对照组(HC)及其他神经退行性疾病(NDD)患者方面具有极高的敏感性和特异性,AUROC值分别可达0.937(95%CL 0.907-0.967)和0.955(95%CL 0.928-0.982)[4]。
3.基于PCR平台精准分型ApoE基因
ApoE基因ε4的携带状态,对AD风险评估及治疗策略制定至关重要。最新研究中,通过万人纵向队列随访,得出ApoE ε4等位基因与痴呆风险的关系。到85岁时发展为MCI(轻度认知功能障碍)或痴呆的“终身风险”:不携带ε4(10%~15%)、携带一个ε4(20%~25%)、携带两个ε4(30%~55%)[5]。此外,ApoE ε4等位基因与Aβ单抗用药后淀粉样蛋白相关影像学异常(ARIA)风险显著相关,在Aβ靶向治疗前进行ApoE ε4基因型检测,有助于评估患者发生ARIA的风险,在启动治疗后适当增加ApoE ε4基因携带患者脑影像学检查频次,有助于监测ARIA风险[6]。
通过整合以上检测项目,AD TANGO™系列产品不仅节约了筛选项目的时间,还大大提高了获取检测结果的效率,更具性价比。相比分别检测各单项指标,综合检测方案节省了近1/4的费用。同时,为了让医生更加直观地理解检测结果,迪安诊断对各项检测结果进行整合,并结合临床信息及文献资料提供了充足的支持建议,辅助临床诊断决策的制定。
助力 AD 早期治疗
辅助个体治疗长程管理,优化治疗决策
早期启动Aβ单抗治疗,对于延缓AD疾病进展具有显著的临床获益。临床试验数据表明,Lecanemab和Donanemab在早期AD患者中均能显著延缓疾病进展。Lecanemab的开放标签延长期(OLE)研究发现,延迟起始治疗的患者获益远不及早期开始治疗者,这进一步强调了早期疾病修饰治疗(DMT)的重要性[7]。Donanemab的III期临床试验也证实,在AD疾病谱的早期阶段,尤其是tau蛋白病理尚未广泛扩散前,是单抗治疗的关键时间窗[8]。
此外,在AD早期阶段,Aβ沉积较少且血脑屏障完整性较强,使用Aβ单抗药物可显著降低ARIA-E(伴有水肿的淀粉样蛋白相关成像异常)事件的发生率。Lecanemab的Clarity AD研究显示,轻度痴呆患者的ARIA-E发生率为27%,而MCI/极轻度痴呆患者仅为1.8%,表明疾病越轻(如MCI阶段),ARIA风险越低[9]。Donanemab的TRAILBLAZER-ALZ 2研究也发现,基线高tau蛋白水平组的ARIA风险更高。因此,越早期启动Aβ单抗治疗,临床获益越大且并发症风险更小[8]。AD早期治疗的先决条件是早期筛查和诊断,AD TANGO™系列产品的推出,为这一目标的实现提供了有力支持。
迪安诊断TANGO中心配置了质谱平台、免疫平台、发光平台、PCR平台、测序平台等多种高精技术平台,致力于神经退行性疾病的精准筛查和诊断,通过组合优势技术平台的不同指标,致力于为临床提供精准诊疗的创新解决方案,推动神经退行性疾病早期预警、病理机制解析及治疗策略的创新研究,以应对老龄化社会带来的挑战。
未来,AD TANGO™系列将推出更多创新解决方案,优化临床决策路径,推动早期精准干预,提升诊疗效率,降低医疗系统负担,并为个体化治疗方案的制定提供科学依据。
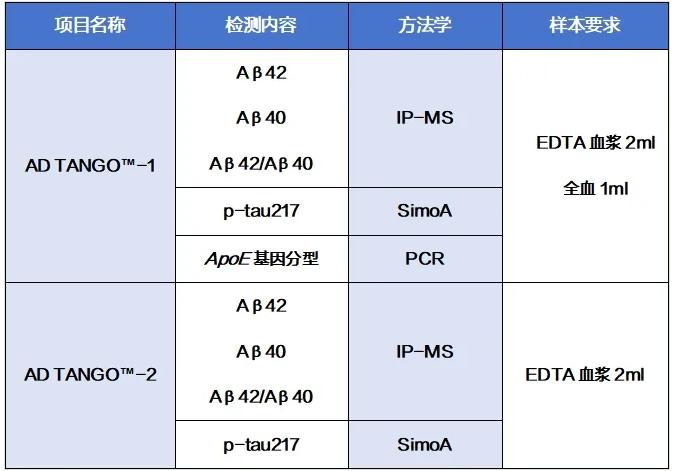
迪安诊断AD TANGO™系列产品检测项目信息
参考文献
1.Jia, J., et al., Biomarker Changes during 20 Years Preceding Alzheimer's Disease. N Engl J Med, 2024. 390(8): p. 712-722.
2.Weber, D.M., et al., A new LC-MS/MS assay for the quantification of Aβ40 and Aβ42 in plasma: validation and clinical performance. Alzheimer's & Dementia, 2022. 18(S6): p. e064182.
3.Wang Y, et al. Clinical utility of plasma Aβ42/Aβ40 ratio measured by LC-MS/MS in Alzheimer's disease assessment: A multicenter study. J Prev Alzheimers Dis 2025;12(4):100065.
4.Pilotto, Andrea et al. Plasma p-tau217 in Alzheimer's disease: Lumipulse and ALZpath SIMOA head-to-head comparison. medRxiv : the preprint server for health sciences, 2024.05.02.24306780. 3 May. 2024,
5.Reiman, E.M., V. Ghisays, and J.B. Langbaum, The Risk of Alzheimer Disease in APOE4 Homozygotes. JAMA Neurol, 2025
6.Cummings, J., et al., Anti-Amyloid Monoclonal Antibodies for the Treatment of Alzheimer's Disease. BioDrugs, 2024. 38(1): p. 5-22.
7.Van Dyck, Christopher H. et al. “Is there Evidence for a Continued Benefit for Long‐Term Lecanemab Treatment? A Benefit/Risk Update from Long‐Term Efficacy, Safety and Biomarker Data.” Alzheimer's & Dementia vol. 20,Suppl 6 e092094. 9 Jan. 2025,
8.Sims JR, Zimmer JA, Evans CD, et al; TRAILBLAZER-ALZ 2 Investigators. Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial. JAMA. 2023 Aug 8;330(6):512-527.
9.Van Dyck C H, Swanson C J, Aisen P, et al. Lecanemab in early Alzheimer’s disease[J]. New England Journal of Medicine, 2023, 388(1): 9-21.





