近日,浙江大学医学院附属邵逸夫医院妇科与迪安诊断合作的研究成果,在国际期刊《BMC Cancer》(2024年IF=3.4)上发表。该研究应用迪安诊断临床基因组中心二代测序 (NGS) 平台,对遗传性卵巢癌的基因突变谱进行系统性分析,并探究新的致病基因。

论文发布截图,点击文末“阅读原文”查阅全文
研究背景
卵巢癌作为死亡率最高的妇科恶性肿瘤,严重威胁女性的生命健康。卵巢癌具有一定的遗传性和家族聚集性,约10%至20%的病例与自身携带特定基因的胚系突变(即生殖细胞中存在的、可遗传的基因突变)有关[1]。
目前,已发现有多种遗传易感基因与卵巢癌相关,其中最著名的是BRCA1和BRCA2,其致病变异的携带者,终生患卵巢癌风险分别约为54%和32%[2]。携带某些遗传性卵巢癌易感基因(如BRCA1/2、林奇综合征相关基因MLH1、MSH2等)的个体,亦可能面临患其他癌症(如乳腺癌和子宫内膜癌)的风险。
随着二代测序 (NGS) 技术的发展,研究者能够同时分析与遗传性卵巢癌相关的多个基因,识别罕见的胚系变异,并可能在高风险家庭中发现新的肿瘤易感基因。本研究采用NGS技术中的全外显子组测序 (WES) 技术,调查了大样本中国卵巢癌患者的胚系变异,旨在识别遗传性卵巢癌的新致病变异,并揭示潜在的新易感基因。
研究方法
本研究纳入了92名经病理确诊的卵巢癌患者,从其外周血提取DNA进行全外显子组测序。基于测序数据,重点分析了12个经典卵巢癌易感基因(ATM、BRCA1、BRCA2、BRIP1、EPCAM 3'缺失、MLH1、MSH2、MSH6、PALB2、PMS2、RAD51C、RAD51D),以及OMIM数据库中其他肿瘤相关的易感基因。根据最终检测结果,将患者分为3类:
阳性组:在12个经典卵巢癌易感基因中,检出致病或可能致病变异。
临床意义未明组:在12个经典卵巢癌易感基因中,仅检出临床意义未明变异,或在其他肿瘤易感基因中检出致病、可能致病及临床意义未明变异。
阴性组:未在任何肿瘤易感基因中,检出致病、可能致病及临床意义未明变异。
研究结果
92名患者中,26例 (28.26%) 在经典卵巢癌易感基因中,检出致病或可能致病变异;24例 (26.09%) 仅在经典卵巢癌易感基因中,或其他肿瘤易感基因中,检出不确定意义变异 (VUS);42例 (45.65%) 未检测到任何相关变异。
在92名患者中,共检测到62个变异。检出率最高的基因依次为:BRCA1 (35%)、BRCA2 (22%)、RAD51D (8%)、ATM (6%)、BRIP1 (6%)和MLH1 (6%)。
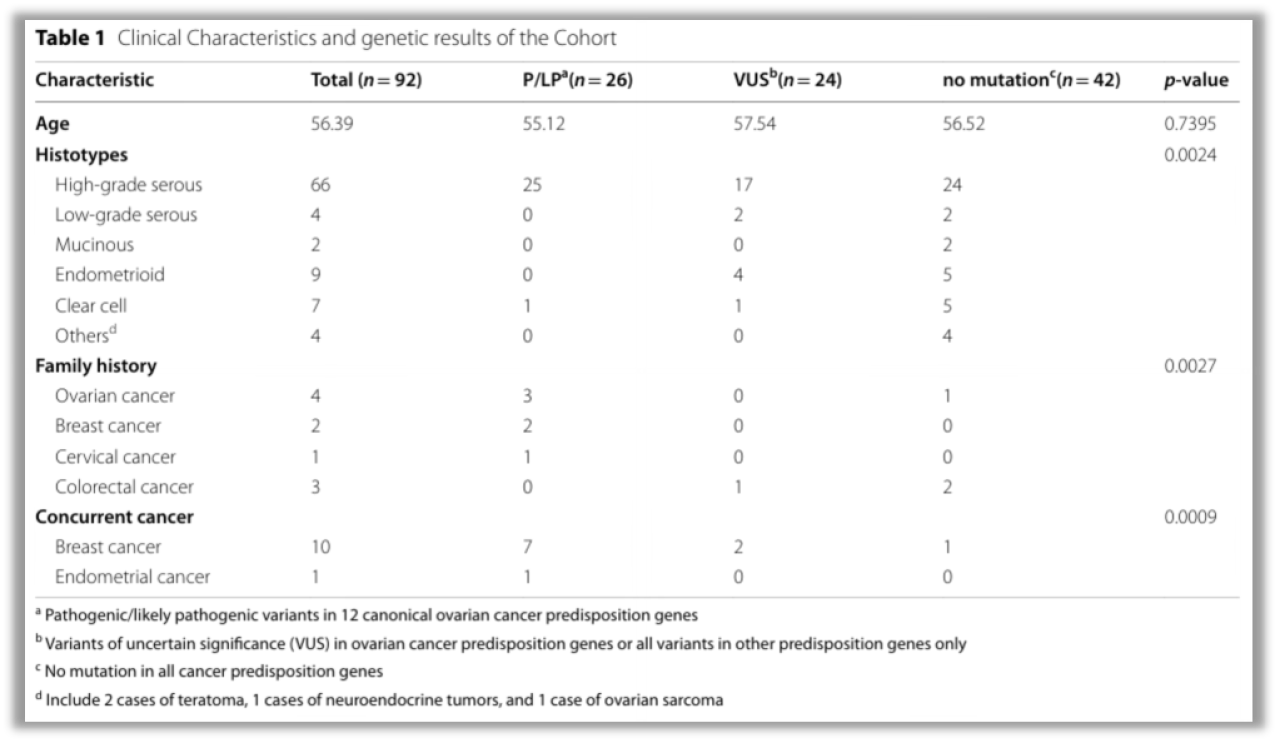
队列的临床特征和遗传结果
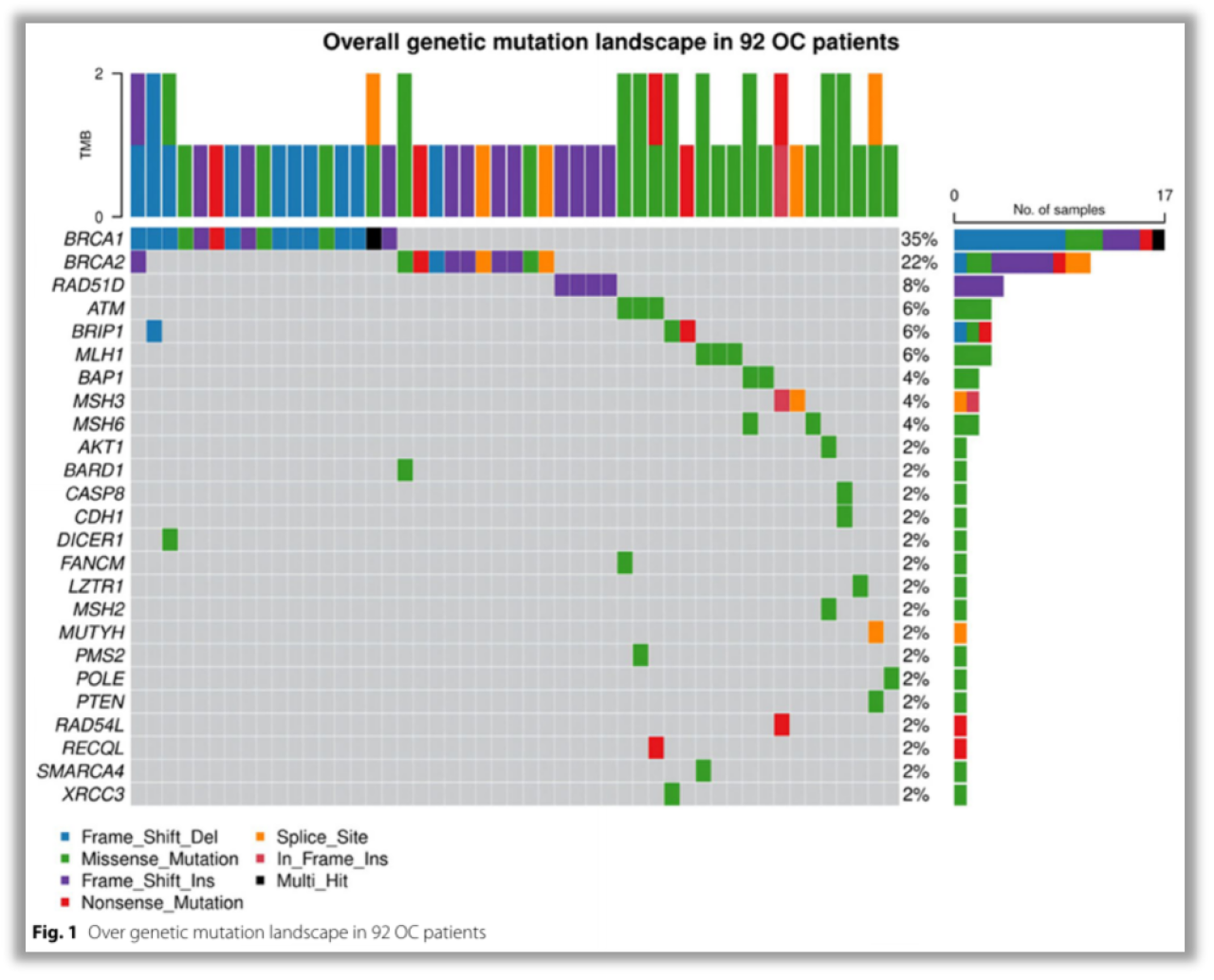
92例卵巢癌患者的基因突变景观
阳性组、临床意义未明组、阴性组三组患者的平均年龄分别为55.12岁、57.54岁和56.52岁,年龄分布无显著差异 (P=0.7395)。三组患者有恶性肿瘤家族史的比例分别为23.08% (6/26)、4.16% (1/24) 和7.14% (3/42)。三组患者伴随其他恶性肿瘤的比例分别为28.57% (8/26)、8.33% (2/24) 和2.38% (1/42)。恶性肿瘤家族史(P=0.0027) 和个人其他恶性肿瘤史 (P=0.0009) 显示与遗传性卵巢癌具有明显相关性。
在26名具有致病或可能致病变异的患者中,25名经病理确诊为高分化浆液性癌 (HGSC),1名为透明细胞癌 (CCC)。HGSC患者中,携带胚系致病变异比例为38.71% (25/62),显著高于其他组织学亚型 (P=0.0024)。
针对美国国立综合癌症网络 (NCCN) 推荐检测的12个经典卵巢癌易感基因,共在26名患者中检测到28个胚系致病或可能致病变异,分别为:BRCA1 (n=13)、BRCA2 (n=8)、RAD51D (n=4)、BRIP1 (n=2)、MSH2 (n=1)。携带MSH2变异的患者同时患有子宫内膜癌,提示为林奇综合征。
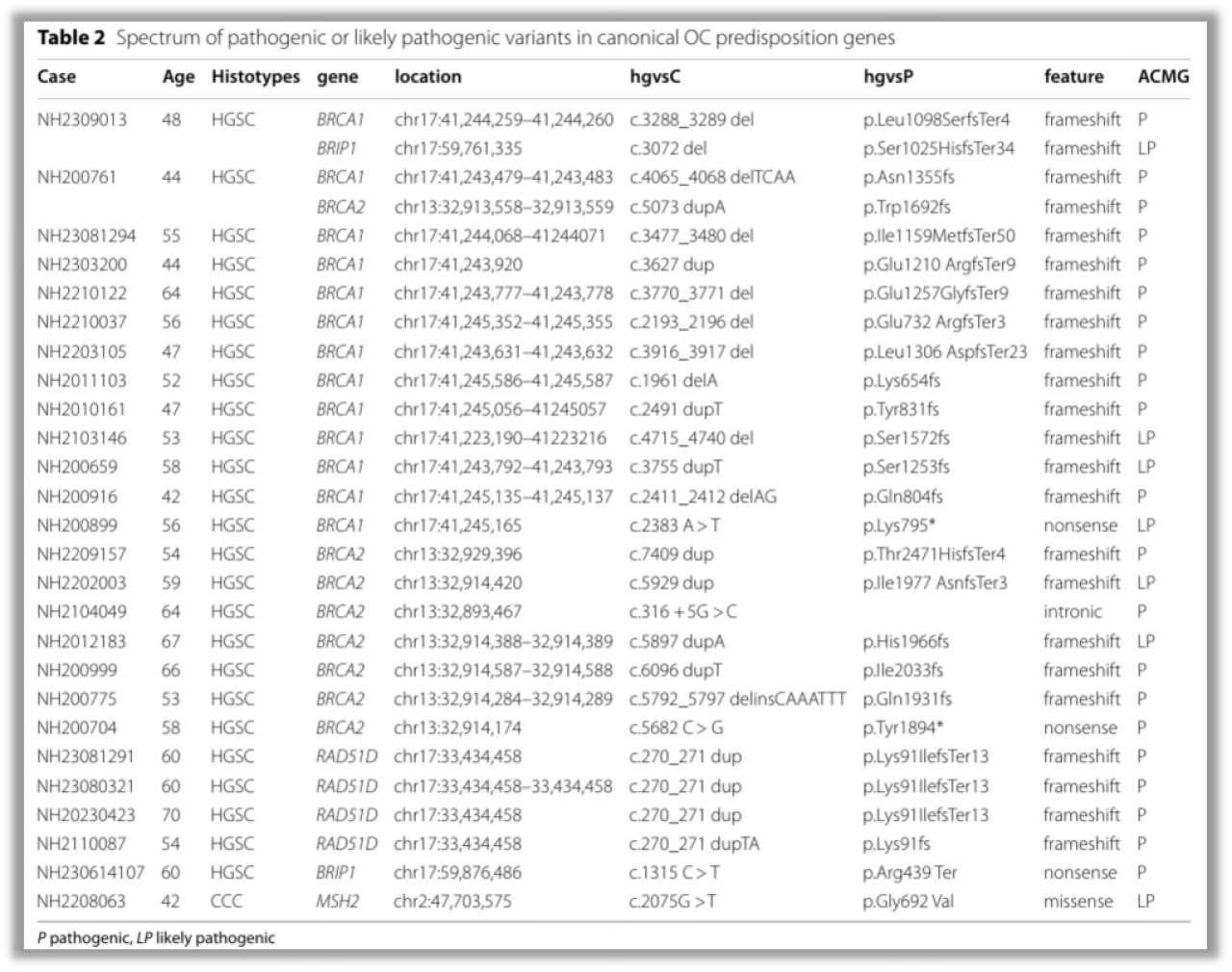
典型卵巢癌易感基因中的致病性或可能致病性变异谱
研究中还鉴定出6个文献及数据库未报道过的新变异,分别为:
NM_007294.4 (BRCA1): c.4715_4740del (p.Ser1572fs)
NM_007294.4 (BRCA1):c.3755dup (p.Ser1253fs)
NM_007294.4 (BRCA1):c.2383A>T (p.Lys795Ter)
NM_000059.4 (BRCA2): c.5929dup (p.Ile1977AsnfsTer3)
NM_000059.4 (BRCA2): c.5897dup (p.His1966fs)
NM_032043.3 (BRIP1): c.3072del (p.Ser1025HisfsTer34)
此外,在经典卵巢癌易感基因中,检测到18个临床意义未明变异,包括ATM (n=3)、BRCA1 (n=5)、BRCA2 (n=3)、BRIP1 (n=1)、MLH1 (n=3)、MSH6 (n=2) 和PMS2 (n=1)。
在其他肿瘤易感基因中,共检测到16个变异,包括BAP1 (n=2)、BARD1 (n=1)、CASP8 (n=1)、CDH1 (n=1)、FANCM (n=1)、LZTR1 (n=1)、MSH3 (n=2)、NBEAL1 (n=1)、POLE (n=1)、PTEN (n=1)、RAD54L (n=1)、RECQL (n=1)、SMARCA4 (n=1) 和XRCC3 (n=1)。识别出11个错义变异、1个内含子变异、1个框内插入变异和3个无义变异。
三个功能丧失变异被识别,包括NM_001142548.1 (RAD54L): c.1825C>T (p.Arg609Ter)、NM_002907.3 (RECQL):c.796C>T (p.Gln266Ter)和NM_001114132.2 (NBEAL1):c.5837dup (p.Tyr1946Ter)。且三名患者均具有遗传性卵巢癌的典型特征,包括双侧卵巢癌、卵巢癌并发子宫内膜癌、卵巢癌并发乳腺癌,提示相关变异可能为患者的病因。
研究小结
在对92名卵巢癌患者进行全外显子组测序 (WES) 的队列研究中,我们在28.26%的病例中识别到了致病或可能致病变异,高于目前已知的遗传性卵巢癌的比例。本研究不仅确认了NCCN推荐的经典卵巢癌易感基因的重要性,还揭示了其他潜在的遗传性卵巢癌易感基因:RAD54L、RECQL和NBEAL1,未来可进一步在更多患者中进行相关基因的验证以及功能学实验。WES显著提高了遗传性卵巢癌患者的检出率,为卵巢癌的遗传基础提供了新的见解。
参考文献
[1]Ponti G, De Angelis C, Ponti R, Pongetti L, Losi L, Sticchi A, et al. Hereditary breast and ovarian cancer: from genes to molecular targeted therapies. Crit Rev Clin Lab Sci. 2023;60(8):640–50.
[2]Petrucelli N, Daly MB, Pal T. BRCA1- and BRCA2-Associated Hereditary Breast and Ovarian Cancer. In: Adam MP, Feldman J, Mirzaa GM, Pagon RA, Wallace SE, Bean LJ, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993 [cited 2024 Mar 1]. Available from: http://www.ncbi.nlm.nih.gov/books/NBK1247/





